리메드, 우울증 치료목적기기 FDA 510K 승인
"미국시장 'ALTMS' 론칭 앞당겨질 것…해외 주요 국가 마케팅 강화"
박기훈 기자
| pkh@newsprime.co.kr |
2022.04.08 10:09:28
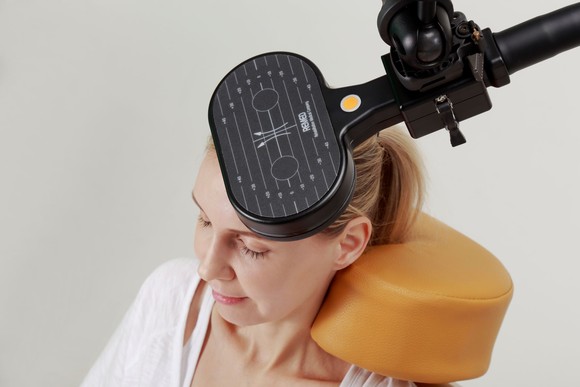
우울증 치료목적용 기기 'ALTMS' ⓒ 리메드
[프라임경제] 전자약 전문 기업 리메드(302550)가 지난 6일 미국 식품의약국(FDA)으로부터 우울증 치료목적용 기기 'ALTMS'의 Special 510(K)(시판 전 신고) 허가를 승인 받았다고 밝혔다.
회사 관계자는 "2021년 5월 만성통증 치료용 신경자기자극장비 'Talent-Pro'가 미국 FDA에서 공식 승인돼 미국 시판허가를 획득한 바 있으며 같은해 11월 비침습적방법으로 뇌질환 치료·재활 목적용인 경두개자기자극기기 'ALTMS'에 대해 미국 FDA 승인을 획득한 바 있다"고 설명했다.
이어 "2022년에 들어서 또 다시 FDA 승인을 받아낸 것은 지속적으로 제품의 성능과 기능을 업그레이드 하는 연구개발을 지속하는 것을 반영한 것"이라고 덧붙였다.
고은현 리메드 대표는 "정확한 시점은 확정되지 않았지만 이번 최종 승인으로 미국시장에서 'ALTMS' 론칭이 앞당겨질 것"이라며 "올해는 해외 주요 국가에 대한 마케팅을 더욱 강화할 것"이라고 말했다.
한편 'ALTMS' 제품은 현재 국내 및 유럽 시장에서 이미 검증이 완료됐으며 우울증 외에 추가적인 적응증 확대를 위한 임상이 지속적으로 진행 중에 있다.
ⓒ 프라임경제(http://www.newsprime.co.kr) 무단전재 및 재배포금지




























![[포토] '잊혀진 전사의 조선신파, 그리고 피네간의 경야' 이상현 작가 개인전](https://www.newsprime.co.kr//data/cache/public/photos/cdn/20250831/art_698548_1754010586_245x140.jpg)




